


0
из 10Решил заданий
0
из 10Не решил заданий
10
из 10Осталось заданий
Формат ответа: цифра или несколько цифр, слово или несколько слов. Вопросы на соответствие "буква" - "цифра" должны записываться как несколько цифр. Между словами и цифрами не должно быть пробелов или других знаков.
Примеры ответов: 7 или здесьисейчас или 3514
Установление молекулярной и структурной формулы вещества
10 заданийПри взаимодействии органического вещества массой 14,8 г с металлическим натрием собрали 2,24 л (н.у.) водорода. В ходе исследования химических свойств этого вещества установлено, что при его взаимодействии с оксидом меди (II) образуется кетон. На основании данных условия задания
1) произведите вычисления, необходимые для установления молекулярной формулы органического вещества;
2) установите молекулярную формулу исходного органического вещества;
3) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
4) напишите уравнение реакции этого вещества с оксидом меди (II).
Кетоны образуются при окислении оксидом меди (II) вторичных спиртов, следовательно, неизвестное вещество – вторичный спирт.
Общая формула вещества CxHyOH
1) Составляем уравнение реакции в общем виде и находим количество вещества водорода:
2CxHyOH + 2Na → 2CxHyONa + H2
n(H2) = Vг / VM = 2,24 / 22,4 = 0,1 моль
2) Находим молекулярную формулу спирта:
по уравнению реакции:
n(CxHyOH) = 2*n(H2) = 0,2 моль
М(CxHyOH) = 14,8 / 0,2 = 74 г/моль
вычисляем: х = 4 и у = 9
молекулярная формула спирта C4H9OH
3) Составляем структурную формулу вещества:
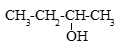
4) Уравнение реакции вещества с оксидом меди (II):

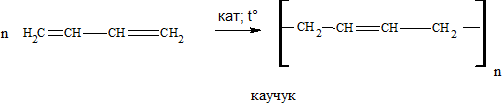
Установите молекулярную формулу диена, относительная плотность паров которого по воздуху 1,862. Установите структурную формулу вещества, если оно известно как синтетический каучук. Запишите реакцию полимеризации
CnH2n-2 – общая формула диенов
M (CnH2n-2) = Dвозд (CnH2n-2) * M (возд) = 1,862 * 29 = 54 г/моль
14n – 2 = 54
14n = 56
n = 4
Вещество C4H6
Структурная формула: CH2-CH=CH-CH2
Некоторая предельная одноосновная карбоновая кислота массой 6 г требует для полной этерификации такой же массы спирта. При этом получается 10,2 г сложного эфира. Установите молекулярную формулу этой карбоновой кислоты. Запишите реакцию этой кислоты со спиртом. Если известно, что спирт в реакции с оксидом меди даёт кетон.
1) Уравнение реакции этерификации в общем виде:
CnH2n+1COOH + ROH → CnH2n+1COOR + H2O
2) Масса и количество вещества воды:
m(H2O) = (6 + 6) – 10,2 = 1,8 г
n(H2O) = 1,8 / 18 = 0,1 моль
3) Формула кислоты:
по уравнению реакции
n(CnH2n+1COOH) = m / n = 6 / 0,1 = 60 г/моль
12n + 2n + 1 + 12 + 16 ∙ 2 + 1 = 60
n = 1
Формула кислоты – CH3COOH
4) 4) Так как спирт и кислота имеют одинаковую массу и реагируют в одинаковом соотношении, то исходный спирт – пропанол-1
$\rm CH_3COOH + CH_3CH_2CH_2OH \overset{H^{+}}{\rightleftharpoons} H_2O + CH_3COOCH_2CH_2CH_3$
В результате окисления 23 г предельного одноатомного спирта оксидом меди (II) получены продукты реакции общей массой 63 г. Определите молекулярную формулу исходного спирта. Запишите реакцию одновременной дегидратации и дегидрирования в присутствии катализаторов и температуры 400°С
1) Уравнение реакции и количество вещества CuO:
CnH2n+1CH2OH + CuO → CnH2n+1CHO + Cu + H2O
По закону сохранения массы
23 + m(CuO) = 63
m(CuO) = 40 г
n(CuO) = 40 / 80 = 0,5 моль
2 ) Рассчитываем молярную массу спирта:
по уравнению реакции
n(спирта) = n(CuO) = 0,5 моль
М(спирта) = 23 / 0,5 = 46 г/моль
3) Определяем формулу спирта:
М(CnH2n+1CH2OH) = 12n + 2n + 1 + 12 + 2 + 16 + 1 = (14n + 32) г/моль
14n + 32 = 46
n = 1
Формула спирта – CH3CH2OH или C2H5OH
4 )В таких условиях протекает реакция Лебедева с образованием бутадиена-1,3
$\rm 2C_2H_5-OH \overset{\text{кат}, t^{\circ}}{\longrightarrow} \underset{\text{бутадиен - 1,3}}{\chemfig{H_2C=CH-CH=CH_2}} + 2H_2O + H_2$
Определите молекулярную формулу алкена, если известно, что одно и то же количество его, взаимодействуя с различными галогенами, образует соответственно или 5,23 г хлорпроизводного, или 8,2 г бромпроизводного. Запишите реакцию взаимодействия данного алкена с водным раствором перманганата калия при 0°С
1) Уравнения реакций и соотношение реагирующих веществ:
CnH2n + HCl → CnH2n+1Cl(1)
CnH2n + HBr → CnH2n+1Br(2)
n(CnH2n+1Cl) = n(CnH2n+1Br) = n(CnH2n)
2) Рассчитываем количество вещества хлор- и бромпроизводных:
n(CnH2n+1Cl) = 5,23 / (12n + 2n + 1 + 35,5) = 5,23 / (14n + 36,5) моль
n(CnH2n+1Br) = 8,2 / (12n + 2n + 1 + 80) = 8,2 / (14n + 81) моль
3) Находим индекс «n» и формулу алкена:
5,23 / (14n + 36,5) = 8,2 / (14n + 81)
n = 3, алкен C3H6
4)
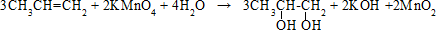
При взаимодействии органического вещества массой 14,8 г с металлическим натрием собрали 2,24 л (н. у.) водорода. В ходе исследования химических свойств этого вещества установлено, что при его взаимодействии с оксидом меди(II) образуется кетон.
1. установите простейшую молекулярную формулу соединения,
2. составьте его структурную формулу,
3. приведите уравнение реакции этого вещества с оксидом меди (II)
|
Содержание ответа |
Баллы |
|
Вариант ответа: Общая формула вещества: CxHyOH 1) Составляем урвнение реакции в общем виде и находим количество водорода 2 CxHyOH + 2 Na → 2CxHyONa + H2 n(H2) = 2, 24/22,4 = 0,1моль 2) Находим молекулярную формулу спирта по уравнению рекции: n(CxHyOH) = 2n(H2) = 0,2моль M(CxHyOH) = 14,8/0,2 = 74г/моль Вычисляем х=4 и у=9 Молекулярная формула спирта: С4Н9ОН Структурная формула: |
|
|
Ответ правильный и полный, содержит следующие элементы:
|
3 |
|
Правильно записаны два элемента ответа |
2 |
|
Правильно записаны один элемент ответа |
1 |
|
Все элементы ответа записаны неверно |
0 |
|
Максимальный балл |
3 |
При сжигании образца некоторого органического соединения массой 29,6 г получено 70,4 г углекислого газа и 36,0 г воды. Известно, что относительная плотность паров этого вещества по воздуху равна 2,552. В ходе исследования химических свойств этого вещества установлено, что при взаимодействии этого вещества с оксидом меди(II) образуется кетон.
1. установите простейшую молекулярную формулу соединения,
2. составьте его структурную формулу,
3. запишите уравнение реакции данного соединения с оксидом меди(II).
|
Содержание ответа |
Баллы |
|
Вариант ответа: Общая формула вещества: CxHyOz n(CO)=70.4/44 = 1.6 моль n(C) = 1.6 моль n(H2O) = 36/18 = 2 моль n(H) = 2*2 = 4 моль m(O) = 29.6-1.6*12-4 = 6.4 n(O) = 0.4
x : y : z 1,6:4:0,4 4 : 10 : 1
Молярная масса вещества: M(CxHyOz) = 37*2 = 74 г/моль C4H10O – молекулярная формула CH3-CH(OH)-CH2-CH3 – структурная формула CH3-CH(OH)-CH2-CH3 + CuO = CH3-C(O)-CH2-CH3 + Cu + H2O |
|
|
Ответ правильный и полный, содержит следующие элементы:
|
3 |
|
Правильно записаны два элемента ответа |
2 |
|
Правильно записаны один элемент ответа |
1 |
|
Все элементы ответа записаны неверно |
0 |
|
Максимальный балл |
3 |
Некоторое органическое соединение массой 5,8 г, взаимодействуя с гидроксидом меди(II), при нагревании образовало 14,4 г осадка оксида меди(I). Указанное органическое соединение вступает в реакции присоединения гидросульфита натрия и этанола.
1. установите простейшую молекулярную формулу соединения
2. составьте его структурную формулу,
3. приведите уравнение реакции, описанное в задаче.
|
Содержание ответа |
Баллы |
|
Вариант ответа: Вещество, взаимодействующее с гидроксидом меди(II) с образованием Cu2O, вступающее в реакции присоединения с гидросульфитом натрия и этанола, относится к классу альдегидов. Общая формула CnH2nO.
Из уравнения следует, что n(CnH2nO) = n (CuO2) 5,8/M=14,4/144 M(альдегида)= 58г/моль Решай уравнение для молярной массы получим: М = 12n +2n +16 = 14n +16 14n +16 = 58 n = 3
|
|
|
Ответ правильный и полный, содержит следующие элементы:
|
3 |
|
Правильно записаны два элемента ответа |
2 |
|
Правильно записаны один элемент ответа |
1 |
|
Все элементы ответа записаны неверно |
0 |
|
Максимальный балл |
3 |
При сгорании 16,2 г органического вещества нециклического строения получено 26,88 л углекислого газа (н.у.) и 16,2 г воды. Найдите формулу вещества, если известно, что 1 моль этого вещества может присоединить только 1 моль воды и не вступает в реакцию с аммиачным раствором оксида серебра. На сновании этих данных:
1. установите простейшую молекулярную формулу соединения,
2. составьте его структурную формулу,
3. приведите уравнение реакции вещества с водой.
|
Содержание ответа |
Баллы |
|
Вариант ответа: Общая формула вещеста – CxHyOy n(CO2) = 26,88/22,4 = 1,2 моль, n(C) = 1,2 моль m(C) = 14,4г n(H2O) = 16,2/18 = 0,9 моль, n(H) = 0,9*2 = 1,8 моль m(H) = 1,8 m(O) = 16,2 – 14,2 – 1,8 = 0 Определяем молекулярную формулу вещества n(C):C(H) : = 1,2 : 1,8= 1:2 = 2:4 => простейшая формула C2H4 СH2=CH2 CH2=CH2 + H2O = CH3 – CH2 – OH |
|
|
Ответ правильный и полный, содержит следующие элементы:
|
3 |
|
Правильно записаны два элемента ответа |
2 |
|
Правильно записаны один элемент ответа |
1 |
|
Все элементы ответа записаны неверно |
0 |
|
Максимальный балл |
3 |
При сжигании 0,45 г газообразного органического вещества выделилось 0,448 л (н. у.) углекислого газа, 0,63 г воды и 0,112 л (н. у.) азота. Плотность вещества по азоту 1,607. В ходе исследования химических свойств этого вещества установлено, что при его взаимодействии с азотистой кислотой выделяется азот.
1. установите простейшую молекулярную формулу соединения,
2. составьте его структурную формулу,
3. приведите уравнение реакции этого вещества с азотистой кислотой
|
Содержание ответа |
Баллы |
|
Вариант ответа:
CxHyOzNu – общая формула
1) M(CxHyOzNu)=DN2(CxHyOzNu)*M(N2)=1,607*28г/моль=45г/моль n(CO2)=V/VM=0,448л/(22,4л/моль)=0,02моль С => CO2 1 моль 1 моль n(C)=n(CO2)=0,02 моль m(C)=0,02моль*12г/моль=0,24г б) n(N2)=0,112л/(22,4л/моль)=5ммоль 2N=>N2 2 моль 1 моль n(N)=2n(N2)=0,01моль m(N)=0,01моль*14г/моль=0,14г n(H2O)=0,63г/(18г/моль)=0,035моль 2H => H2 2 моль 1 моль n(H)=2n(H2)=0,07моль m(H)=0,07моль*1г/моль=0,07г m(N)+m(H)+m(С)=m(CxHyOzNu)
2) Определение формулы вещества x:y:u=n(C):n(H):n(N) x:y:u=0,02:0,07:0,01; x:y:u=2:7:1 Простейшая формула вещества-C2H7N Mпрост.=Mист. => Молекулярная формула = простейшей формуле
Структурная формула: СH3-CH2-NH2 C2H7N + HNO2 = C2H5OH + N2 + H2O |
|
|
Ответ правильный и полный, содержит следующие элементы:
|
3 |
|
Правильно записаны два элемента ответа |
2 |
|
Правильно записаны один элемент ответа |
1 |
|
Все элементы ответа записаны неверно |
0 |
|
Максимальный балл |
3 |

Решено верно

Решено верно

Решено верно

Решено верно

Решено верно

Решено верно

Решено верно

Решено верно

Решено верно

Решено верно

Решено верно

Решено верно

«Выбери тест, предмет и нажми кнопку «Начать решать»
После выбора предмета необходимо выбрать на вкладке задания, варианты ЕГЭ, ОГЭ или другого теста, или теорию
Решай задания и записывай ответы. После 1-ой попытки ты сможешь посмотреть решение
Сбоку ты можешь посмотреть статистику и прогресс по предмету
Нажми, чтобы начать решать вариант. Как только ты перейдешь на страницу, запустится счетчик времени, поэтому подготовь заранее все, что может тебе понадобиться

Отмечай те статьи, что прочитал, чтобы было удобнее ориентироваться в оглавлении

Ты прошел обучение! Теперь ты знаешь как пользоваться сайтом и можешь переходить к решению заданий